Il Lipedema
Riconosciuta dall’OMS nel 2018, il Lipedema o Lipoedema [British/Australian Spelling] o Lipödem [German Spelling], è una patologia genetica infiammatoria, cronica, degenerativa e invalidante del Tessuto Connettivo Lasso (LCT: Loose Connective Tissue), che provoca un aumento progressivo, fibrotico e deturpante del tessuto adiposo, spesso accompagnato da edema, infiammazione sistemica e dolore. Se trascurata può portare anche a severi quadri di disabilità.
Nota anche come lipoipertrofia simmetrica dolorosa delle estremità, lipalgia, lipoiperplasia dolorosa, sindrome del grasso doloroso, sindrome di Allen e Hines (dai nomi di coloro che la descrissero per primi alla Mayo Clinic negli anni ’40), o lipodistrofia ipertrofica dolorosa, la malattia colpisce maggiormente il Tessuto Adiposo Sottocutaneo (SAT: Subcutaneous Adipose Tissue), con maggiore incidenza in alcuni distretti corporei, ma essa interessa tutto il tessuto connettivo, la fascia muscolare e il sistema linfatico e vascolare. La malattia è scarsamente conosciuta e anche nel mondo sanitario è spesso confusa con altre patologie come l’obesità indotta dallo stile di vita o con l’obesità ginoide e adiposità localizzata, con il linfedema e persino con altre condizioni di pertinenza cosmetologica (inestetismi come la panniculopatia edemato-fibro-sclerotica, comunemente “cellulite”). Il lipedema può essere primario o sindromico. Le forme sindromiche sono quelle che presentano maggiori difficoltà diagnostiche.
In passato il lipedema veniva classificato come un disordine degli adipociti (Fat Disorder) o una patologia relativa al solo tessuto adiposo sottocutaneo e inserita nella classificazione ICD 10 tra le lipomatosi non altrimenti specificate dei disordini metabolici (ICD-10 E88.2). Attualmente possiede un codice ICD 11 tra i disordini non infiammatori del tessuto adiposo sottocutaneo (ICD 11 EF02.2). Tuttavia la ricerca più recente è incline a descrivere il lipedema come una malattia del tessuto connettivo lasso, in modo da chiarire che essa coinvolge non solo gli adipociti, ma anche tutte le strutture di supporto agli stessi e altre componenti.

Il lipedema colpisce quasi esclusivamente il sesso femminile. Rarissimi, ma comunque presenti e descritti in letteratura, i casi di lipedema maschile (gli uomini sono comunque portatori e possono trasmettere la malattia). Tra le malattie che interessano prevalentemente il tessuto adiposo sottocutaneo il lipedema è la più diffusa e rappresenta un sottogruppo dei disordini dell’adipofascia, costituito dalle patologie RAD (Rare Adipose Disorders masquerading as obesity), di cui fanno parte il DD (Dercum Disease – o Malattia di Dercum), FML (Familial Multiple Lipomatosis), angiolipomatosis e MSL (Multiple Symmetric Lipomatosis).
Il lipedema è una patologia cronica, sottostimata, multifattoriale e fortemente disabilitante fisicamente e psicologicamente. In letteratura è descritta come malattia genetica (codice OMIM 614103) con ereditarietà autosomica dominante a penetranza incompleta o oligogenica, influenzata dai cambiamenti ormonali femminili ed è caratterizzata da un progressivo, abnorme, simmetrico, nodulare e doloroso aumento del tessuto adiposo non rispondente ai comuni meccanismi di regolazione dell’adipostato ipotalamico, soprattutto a carico di alcuni distretti corporei (principalmente fianchi, bacino, arti inferiori e superiori, addome, ma può essere presente in tutto il corpo, anche nel cuoio capelluto), con conseguente deformazione morfologica e sproporzione patognomonica della parte inferiore del corpo (per gli arti a colonna o lobulare) e infiammazione sistemica, anche documentabile da alterazione dei marcatori della flogosi.
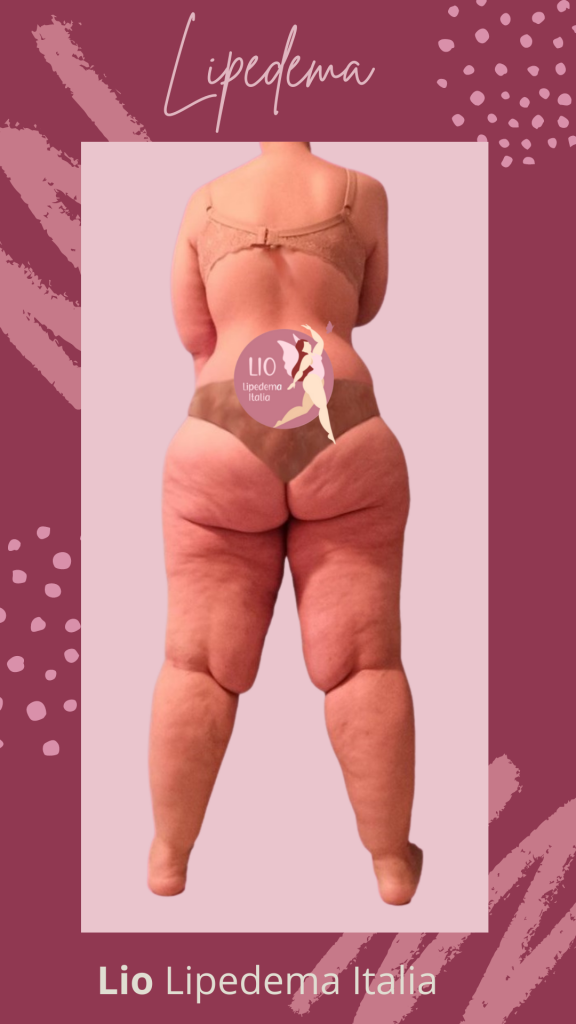
Il grasso nel lipedema può essere estremamente doloroso e difficile da perdere attraverso la dieta, l’esercizio fisico. Il grasso fibrotico (Lipedema FAT) non si riduce in maniera significativa nemmeno dopo la chirurgia bariatrica. I pazienti che presentano obesità in comorbidità possono tuttavia rispondere adeguatamente ai trattamenti di controllo del peso per la componente non fibrotica (Non-Lipedema Fat)
L'aumento di volume nei distretti corporei maggiormente colpiti, unito alla componente del dolore, può limitare severamente la mobilità del paziente
Le CAUSE del lipedema sono ancora oggetto di studio. Di recente è stato isolato il primo gene responsabile in una famiglia affetta da lipedema primario non sindromico in cui si è osservata la mutazione del gene Aldo-Keto Reductase 1C1 (AKR1C1). La ricerca genetica prosegue nell’individuazione di un pannello multi-gene per identificare varianti genetiche predisponenti.
La malattia non è legata a disturbi del comportamento alimentare e non è autodeterminata dal paziente attraverso condotte alimentari poco sane o stili di vita scorretti, anche se ancora oggi buona parte della comunità scientifica che ignora la patologia e la non rispondenza della stessa ai comuni trattamenti dietoterapici, seguita ad approcciarsi alla malattia in questo modo, con gravi conseguenze per il benessere psicofisico degli affetti.
L’eziopatogenesi non è ancora del tutto compresa in tutti i suoi aspetti. Tuttavia l’osservazione clinica suggerisce una commistione di fattori genetici (si osserva familiarità da decenni), influenze ormonali, vasi sanguigni e linfatici dilatati, e infiammazione.
I modelli fisiopatologici più recenti e aggiornati suggeriscono che il lipedema sia un disordine estrogeno-dipendente del tessuto adiposo, attivato da una disfunzione della caveolina 1 (CAV1), una proteina integrale di membrana implicata in numerose segnalazioni mitogeniche, nella tumorigenesi, nella angiogenesi e nella aterosclerosi, in patologie neurodegenerative e nella senescenza, che regola l’endocitosi della MEC (Matrice Extra Cellulare) e da un conseguente disaccoppiamento dei meccanismi di feedback tra CAV1, la metalloproteinasi della matrice MMP14 e i recettori degli estrogeni. Inoltre la ridotta attività della CAV1 sembra avere un ruolo anche nella ridotta funzionalità del sistema linfatico attraverso l’attivazione di ERα e il fattore di trascrizione prospero homeobox 1 (PROX1). La risultante sovraregolazione di questi fattori potrebbe spiegare efficacemente le principali caratteristiche note del lipedema, come l’ipertrofia adiposa, la disfunzione dei vasi sanguigni e linfatici, la complessiva estrogeno-dipendenza (con il relativo dimorfismo sessuale associato), e la compliance meccanica del tessuto adiposo.
La microangiopatia è uno dei cambiamenti più precoci che si osservano nel tessuto adiposo dei malati di lipedema e dal punto di vista immunoistochimico sono stati rilevati infiltrati di macrofagi e proliferazione di cellule progenitrici che suggeriscono come il possibile meccanismo che porta allo sviluppo del lipedema possa includere un’aumentata lipogenesi, che comporta ipossia tissutale, necrosi adipocitaria ed infiltrato infiammatorio che contribuisce alla patogenesi del dolore. Oltre al dolore si associa a edema ortostatico, che peggiora nella seconda parte della giornata e con il clima caldo, ecchimosi, anche spontanee (a causa dell’aumentata permeabilità e fragilità capillare), aumento della sensibilità delle zone affette e parestesie. Frequente la compresenza di ipermobilità articolare sintomatica come da sindrome di HSD (Hypermobility Spectrum Disorder), una variante della sindrome di Ehlers-Danlos, con dati di prevalenza della comorbidità ancora da classificare.
La familiarità è ormai un dato certo e anche studiato ed è fortemente presumibile un’eziologia da squilibrio ormonale che coinvolge principalmente gli estrogeni, in considerazione del fatto che la patologia si manifesta, progredisce e si esacerba in concomitanza delle fasi più significative della vita femminile: pubertà, gravidanza, perimenopausa, chirurgia addominale, assunzione di pillola contraccettiva, trattamenti per la fertilità, patologie a nota eziologia estrogeno-dipendente.
VAI ALLA DIAGNOSI
Il lipedema è una patologia ingravescente, anche quando non associata a patologie correlate. Se trascurato o in assenza di trattamento, può portare anche a severi quadri di disabilità, ipomobilità e dolenzia severa delle zone affette nonché ad alterazioni morfologiche deturpanti, causa di notevole disagio psicologico. Anche negli stadi precoci meno sintomatici la patologia è comunque causa di grave sofferenza psicologica, considerando che si tratta di una patologia fisicamente deturpante nel tempo e l’evolutività della stessa.
Benché non esista una cura definitiva, è possibile sottoporre il paziente a trattamenti sintomatici evidence based in grado di allievarli o di arrestare il quadro evolutivo o quantomeno di rallentarne la progressione. Tali terapie sono mirate al trattamento localizzato dei tessuti, all’asportazione chirurgica del tessuto malato visibile, al trattamento dell’infiammazione sistemica, ma anche in presenza di terapie validate, s’interviene solo su patologia manifesta per alleviare i sintomi più evidenti e con scarse probabilità di prevenzione.
A data odierna in letteratura sono presenti circa 350 articoli sulla patologia, a partire dalla prima descrizione della Mayo Clinic, risalente agli anni 40.
La scarsa conoscenza della patologia comporta un ritardo diagnostico stimato in media di circa 10 anni dall’insorgenza dei sintomi. La diagnosi è clinica ed è fondamentale l’esperienza del medico che effettua la valutazione a fini diagnostici. Gli accertamenti strumentali sono utili per porre diagnosi differenziale con altre patologie. L’attuale quadro assistenziale sui malati italiani è drammatico. La confusione diagnostica altera i dati epidemiologici, che anche in letteratura sono variegati e sottostimati. Cure parziali mutuate da altre patologie vengono somministrate con beneficio temporaneo e la dispersione, la rinuncia e l’abbandono delle cure per mancanza di disponibilità economica è quotidiana.
Guarda la sezione CODICI DEL LIPEDEMA
scopri le video gallery
L’Italia non possiede linee guida nazionali per il trattamento del lipedema. La malattia è menzionata come patologia correlata nelle Linee d’indirizzo ministeriali per il trattamento del linfedema e spesso sono gli specialisti della linfologia a farsi carico di questi pazienti, che provengono nella maggior parte dei casi da un’errata diagnosi di linfedema, ma ai malati di lipedema vengono negate anche le cure che condividono con i malati di queste patologie. Le attuali opportunità di cura nel nostro paese, costantemente limitate dalla disponibilità economica del paziente, provengono da professionisti sanitari pionieri che lottano da anni al fianco dei pazienti e si sono messi a disposizione dell’associazione per fornire aiuto e assistenza e costruire realtà di presa in carico, anche interfacciandosi con colleghi internazionali e nazionali per la costituzione di equipe multidisciplinari ed esercitando la loro professione con la costante frustrazione di non poter erogare le cure necessarie a causa dell’assenza della malattia nei Livelli Essenziali di Assistenza.
I paesi dotati di linee guida e documenti di consenso sono attualmente Germania, Paesi Bassi, Regno Unito, Spagna e di recente anche gli Stati Uniti hanno pubblicato i propri Stardard of Care, al momento i più recenti e aggiornati. La Germania è un paese pioniere che tramite un organismo sanitario governativo (Il DIMDI) ha fatto inserire il lipedema nella versione nazionale della classificazione ICD 10 già diversi anni fa. Ed è l’unico paese al mondo in cui i malati hanno accesso a presidi e terapie riabilitative e in cui i pazienti con malattia avanzata possono essere sottoposti a chirurgia sequenziale in convenzione con la cassa mutua tedesca. Anche il Regno Unito si sta battendo per ottenere i trattamenti a carico del sistema sanitario nazionale. Dalla Spagna arrivano anche importanti novità in campo di trattamento conservativo e chirurgico. Esiste un documento di consenso internazionale in merito alla chirurgia e trattamenti perioperatori e anche il Canada si è dotato di una linea guida per la chirurgia. La Germania resta certamente il paese con il maggior numero di centri di cura specializzati. Le novità statunitensi sono il superamento definitivo del considerare il lipedema come una patologia localizzata e limitata al solo tessuto adiposo, ma di trattarla come affezione di infiammazione sistemica con un approccio globale e olistico e che coinvolge tutto il tessuto connettivo lasso. Diverse assicurazioni sanitarie offrono ormai copertura per le cure specializzate. I contatti con la realtà italiana sono frequenti e sistematici.
Dr Stutz – Lipedema 101- Not All Fat is Created Equal
- Dadras M, Mallinger P, Corterier C, Theodosiadi S, Ghods M (2017) Liposuction in the treatment of lipedema: a longitudinal study. Arch Plast Surg 44(4):324–331
-
Ghods M, Kruppa P (2018) Surgical treatment of lipoedema. Handchir Mikrochir Plast Chir 50(6):400–411
- Kruppa P, Georgiou I, Biermann N, Prantl L, Klein-Weigel P, Ghods M (2020) Lipedema—pathogenesis, diagnosis and treatment options. Dtsch Arztebl Int 117:396–403. https://doi.org/10.3238/arztbl.2020.0396
- Allen EV, Hines EA (1940) Lipedema of the legs: a syndrome characterized by fat legs and orthostatic edema. Proc Staff Mayo Clin 15:184–187
- Buck DW 2nd, Herbst KL (2016) Lipedema: a relatively common disease with extremely common misconceptions. Plast Reconstr Surg Glob Open 4(9):e1043
- Marshall M, Schwahn-Schreiber C (2011) Prävalenz des Lipödems bei berufstätigen Frauen in Deutschland. Phlebologie 40(03):127–134
- Child AH, Gordon KD, Sharpe P et al (2010) Lipedema: an inherited condition. Am J Med Genet A 152a(4):970–976
- Herbst K, Mirkovskaya L, Bharhagava A, Chava Y, Te C (2015) Lipedema fat and signs and symptoms of illness, increase with advancing stage. Arch Med 7:1–8
- Torre YS, Wadeea R, Rosas V, Herbst KL (2018) Lipedema: friend and foe. Horm Mol Biol Clin Investig 33(1):1–10
- Bauer AT, von Lukowicz D, Lossagk K et al (2019) New insights on lipedema: the enigmatic disease of the peripheral fat. Plast Reconstr Surg 144(6):1475–1484
- Bauer AT, von Lukowicz D, Lossagk K et al (2019) Adipose stem cells from lipedema and control adipose tissue respond differently to adipogenic stimulation in vitro. Plast Reconstr Surg 144(3):623–632
- AL-Ghadban S, Cromer S, Allen M et al (2019) Dilated blood and lymphatic microvessels, angiogenesis, increased macrophages, and adipocyte hypertrophy in lipedema thigh skin and fat tissue. J Obes 2019:10
- Priglinger E, Wurzer C, Steffenhagen C et al (2017) The adipose tissue-derived stromal vascular fraction cells from lipedema patients: are they different? Cytotherapy 19(7):849–860
- Baumgartner A, Hueppe M, Schmeller W (2016) Long-term benefit of liposuction in patients with lipoedema: a follow-up study after an average of 4 and 8 years. Br J Dermatol 174(5):1061–1067
- Rapprich S, Dingler A, Podda M (2011) Liposuction is an effective treatment for lipedema-results of a study with 25 patients. J Dtsch Dermatol Ges 9(1):33–40
- Schmeller W, Hüppe M, Meier-Vollrath I (2012) Tumescent liposuction in lipoedema yields good long-term results. Br J Dermatol 166(1):161–168
- Wollina U, Heinig B (2019) Treatment of lipedema by low-volume micro-cannular liposuction in tumescent anesthesia: results in 111 patients. Dermatol Ther 32:e12820
- Bays HE, Chapman RH, Grandy S (2007) The relationship of body mass index to diabetes mellitus, hypertension and dyslipidaemia: comparison of data from two national surveys. Int J Clin Pract 61(5):737–747
- Dudek JE, Bialaszek W, Ostaszewski P, Smidt T (2018) Depression and appearance-related distress in functioning with lipedema. Psychol Health Med 23:1–8
- Halk AB, Habbema L, Genders RE, Hanke CW (2019) Safety studies in the field of liposuction: a systematic review. Dermatol Surg 45(2):171–182
- Iverson RE, Lynch DJ (2004) Practice advisory on liposuction. Plast Reconstr Surg 113(5):1478–1495
- Seretis K, Goulis DG, Koliakos G, Demiri E (2015) Short- and long-term effects of abdominal lipectomy on weight and fat mass in females: a systematic review. Obes Surg 25(10):1950–1958
- Witte T, Dadras M, Heck F et al (2020) Water-jet assisted liposuction for the treatment of lipedema: Standardized treatment protocol and results of 63 patients. J Plast Reconstr Aesthet Surg. https://doi.org/10.1016/j.bjps.2020.03.002
- ISAPS, Global Survey Results (2018) https://www.isaps.org/wp-content/uploads/2019/12/ISAPS-Global-Survey-Results-2018-new.pdf. Visited 01.05.2020
- American Society of Plastic Surgeons, Plastic surgery statistics. https://www.plasticsurgery.org/news/press-releases/new-plastic-surgery-statistics-reveal-trends-toward-body-enhancement. Visited 01.05.2020
- Kruglikov IL, Joffin N, Scherer PE. The MMP14-caveolin axis and its potential
relevance for lipoedema. Nat Rev Endocrinol. 2020 Aug 13. doi:10.1038/s41574-020-0395-z. Epub ahead of print. PMID: 32792644.
- Herbst, K., et al., Lipedema Fat and Signs and Symptoms of Illness, Increase with Advancing Stage. Archives of Medicine, 2015. 7(4:10): p. 1-8.
-
Wold, L.E., E.A. Hines, Jr., and E.V. Allen, Lipedema of the legs; a syndrome characterized by fat legs and edema. Ann Intern Med., 1951. 34(5): p. 1243-50.
-
Bast, J.H., L. Ahmed, and R. Engdahl, Lipedema in patients after bariatric surgery. Surg Obes Relat Dis., 2016. 12(5): p. 1131-2. doi: 10.1016/j.soard.2016.04.013. Epub 2016 Apr 14.
-
Pouwels, S., et al., Lipoedema in patients after bariatric surgery: report of two cases and review of literature. Clin Obes., 2018. 8(2): p. 147-150. doi: 10.1111/cob.12239. Epub 2018 Jan 25.
-
Pouwels, S., et al., Mobility Problems and Weight Regain by Misdiagnosed Lipoedema After Bariatric Surgery: Illustrating the Medical and Legal Aspects. Cureus., 2019. 11(8): p. e5388. doi: 10.7759/cureus.5388.
-
Herbst, K.L., Subcutaneous Adipose Tissue Diseases: Dercum Disease, Lipedema, Familial Multiple Lipomatosis and Madelung Disease, in Endotext, J. Purnell and L. Perreault, Editors. 2019, MDText.com: Massachusetts.
-
Guimberteau, J.-C. and C. Armstrong, Architecture of human living fascia. 2018, United Kingdom: Handspring Publishing, Limited. 204.
-
Bordoni, B., N. Mahabadi, and M. Varacallo, Anatomy, Fascia, in StatPearls [Internet]. 2019, StatPearls Publishing: Treasure Island, Florida.
-
Mulloy, B. and C.C. Rider, Cytokines and proteoglycans: an introductory overview. Biochem Soc Trans., 2006. 34(Pt 3): p. 409-13. doi: 10.1042/BST0340409.
-
Herbst, K.L., C. Ussery, and A. Eekema, Pilot study: whole body manual subcutaneous adipose tissue (SAT) therapy improved pain and SAT structure in women with lipedema. Horm Mol Biol Clin Investig., 2017. 33(2): p. /j/hmbci.2018.33.issue-2/hmbci-2017-0035/hmbci-2017-0035.xml. doi: 10.1515/hmbci-2017-0035.
-
Iker, E., et al., Characterizing Lower Extremity Lymphedema and Lipedema with Cutaneous Ultrasonography and an Objective Computer-Assisted Measurement of Dermal Echogenicity. Lymphat Res Biol, 2019. 7(10).
-
Kreitz, S., et al., Nondestructive method to evaluate the collagen content of fibrin-based tissue engineered structures via ultrasound. Tissue Eng Part C Methods., 2011. 17(10): p. 1021-6. doi: 10.1089/ten.TEC.2010.0669. Epub 2011 Jul 26.
-
Roberts, M.A., et al., Increased Hyaluronan Expression at Distinct Time Points in Acute Lymphedema. Lymphatic Research and Biology, 2012. 10(3): p. 122-128.
-
Zhu, Y., C. Crewe, and P.E. Scherer, Hyaluronan in adipose tissue: Beyond dermal filler and therapeutic carrier. Sci Transl Med., 2016. 8(323): p. 323ps4. doi: 10.1126/scitranslmed.aad6793. Epub 2016 Jan 27.
-
Schneider, M., E.M. Conway, and P. Carmeliet, Lymph makes you fat. Nat Genet., 2005. 37(10): p. 1023-4.
-
Zampell, J.C., et al., Regulation of adipogenesis by lymphatic fluid stasis: part I. Adipogenesis, fibrosis, and inflammation. Plast Reconstr Surg., 2012. 129(4): p. 825-34. doi: 10.1097/PRS.0b013e3182450b2d.
-
Olszewski, W.L., M. Zaleska, and M. Cakala, Lymphedema is more than excess of fluid; a lympho-fibro-adipo-edema. Veins and Lymphatics, 2018. 7: p. 7984.
-
Bertsch, T. and G. Erbacher, Lipoedema – myths and facts Part 1. Phlebologie, 2018. 47: p. 84-92.
-
Bertsch, T., et al., Lipoedema – myths and facts, Part 5. European Best Practice of Lipoedema – Summary of the European Lipoedema Forum consensus. Phlebologie, 2020. 49: p. 31-49.
-
Bhave, G. and E.G. Neilson, Body fluid dynamics: back to the future. J Am Soc Nephrol., 2011. 22(12): p. 2166-81. doi: 10.1681/ASN.2011080865. Epub 2011 Oct 27.
-
Mortimer, P.S. and J.R. Levick, Chronic peripheral oedema: the critical role of the lymphatic system. Clin Med (Lond). 2004. 4(5): p. 448-53. doi: 10.7861/clinmedicine.4-5-448.
-
Jackson, W.F., Microcirculation, in Muscle. Fundamental Biology and Mechanism of Disease, J.A. Hill and E.N. Olson, Editors. 2012, Elsevier Science: Canada.
-
Pober, J.S. and W.C. Sessa, Inflammation and the blood microvascular system. Cold Spring Harb Perspect Biol., 2014. 7(1): p. a016345. doi: 10.1101/cshperspect.a016345.
-
Levick, J.R. and C.C. Michel, Microvascular fluid exchange and the revised Starling principle. Cardiovasc Res., 2010. 87(2): p. 198-210. doi: 10.1093/cvr/cvq062. Epub 2010 Mar 3.
-
Guyton, A.C., Pressure-volume relationships in the interstitial spaces. Invest Ophthalmol., 1965. 4(6): p. 1075-84.
-
Nijst, P., et al., Dermal Interstitial Alterations in Patients With Heart Failure and Reduced Ejection Fraction: A Potential Contributor to Fluid Accumulation? Circ Heart Fail., 2018. 11(7): p. e004763. doi: 10.1161/CIRCHEARTFAILURE.117.004763.
-
Crescenzi, R., et al., Lipedema and Dercum’s Disease: A New Application of Bioimpedance. Lymphat Res Biol, 2019. 13(10).
-
Ward, L., et al., Assessment of bilateral limb lymphedema by bioelectrical impedance spectroscopy. Int J Gynecol Cancer., 2011. 21(2): p. 409-18. doi: 10.1097/IGC.0b013e31820866e1.
-
Torre, Y.S., et al., Lipedema: friend and foe. Horm Mol Biol Clin Investig., 2018. 33(1).(pii): p. /j/hmbci.ahead-of-print/hmbci-2017-0076/hmbci-2017-0076.xml. doi: 10.1515/hmbci-2017-0076.
-
Harwood, C.A., et al., Lymphatic and venous function in lipoedema. Br J Dermatol, 1996. 134(1): p. 1-6.
-
Partsch, H., et al., Clinical use of indirect lymphography in different forms of leg edema. Lymphology, 1988. 21(3): p. 152-60.
-
Beltran, K. and K.L. Herbst, Differentiating lipedema and Dercum’s disease. Int J Obes (Lond). 2017. 41(2): p. 240-245.
-
Malfait, F., et al., The 2017 international classification of the Ehlers-Danlos syndromes. Am J Med Genet C Semin Med Genet., 2017. 175(1): p. 8-26. doi: 10.1002/ajmg.c.31552.
-
Comper, W.D. and T.C. Laurent, Physiological function of connective tissue polysaccharides. Physiol Rev., 1978. 58(1): p. 255-315. doi: 10.1152/physrev.1978.58.1.255.
-
Granger, H.J., et al., Dynamics and Control of Transmicrovascular Fluid Exchange. Edema, 1984. 8: p. 189-224.
-
Wiig, H., K. Rubin, and R.K. Reed, New and active role of the interstitium in control of interstitial fluid pressure: potential therapeutic consequences. Acta Anaesthesiol Scand., 2003. 47(2): p. 111-21. doi: 10.1034/j.1399-6576.2003.00050.x.
-
Crescenzi, R., et al., Tissue Sodium Content is Elevated in the Skin and Subcutaneous Adipose Tissue in Women with Lipedema. Obesity (Silver Spring). 2018. 26(2): p. 310-317. doi: 10.1002/oby.22090. Epub 2017 Dec 27.
-
Reed, R.K. and K. Rubin, Transcapillary exchange: role and importance of the interstitial fluid pressure and the extracellular matrix. Cardiovasc Res., 2010. 87(2): p. 211-7. doi: 10.1093/cvr/cvq143. Epub 2010 May 13.
-
AL-Ghadban, S., et al., Dilated Blood and Lymphatic Microvessels, Angiogenesis, Increased Macrophages, and Adipocyte Hypertrophy in Lipedema Thigh Skin and Fat Tissue. Journal of Obesity, 2019.
-
Foldi, E. and M. Foldi, Lipedema, in Foldi’s Textbook of Lymphology, M. Foldi and E. Foldi, Editors. 2006, Elsevier GmbH: Munich, Germany. p. 551.
-
Suga, H., et al., Adipose tissue remodeling in lipedema: adipocyte death and concurrent regeneration. J Cutan Pathol, 2009. 3: p. 3.
-
Bacci, P.A. and G. Liebaschoff, Clinical-Therapeutic Classification: BIMED-TCD, in Cellulite. Pathophysiology and Treatment, M.P. Goldman, et al., Editors. 2006, Taylor & Francis Group: New York. p. 115-141.
-
Lotti, T., et al., Proteoglycans in so-called cellulite. Int J Dermatol., 1990. 29(4): p. 272-4. doi: 10.1111/j.1365-4362.1990.tb02560.x.
-
Fife, C.E., E.A. Maus, and M.J. Carter, Lipedema: a frequently misdiagnosed and misunderstood fatty deposition syndrome. Adv, 2010. 23(2): p. 81-92; quiz 93-4.
-
Priglinger, E., et al., The adipose tissue-derived stromal vascular fraction cells from lipedema patients: Are they different? Cytotherapy., 2017. 19(7): p. 849-860. doi: 10.1016/j.jcyt.2017.03.073. Epub 2017 Apr 25.
-
Bacci, P.A. and G. Leibaschoff, Pathophysiology of Celulite, in Cellulite. Pathophysiology and Treatment, M.P. Goldman, et al., Editors. 2006, Taylor % Francis Group: New York. p. 69.
-
Fatourechi, V., Pretibial myxedema: pathophysiology and treatment options. Am J Clin Dermatol, 2005. 6(5): p. 295-309. doi: 10.2165/00128071-200506050-00003.
-
Drubaix, I., et al., [Role of glycosoaminoglycans in venous disease. Mode of action of some flavonoid drugs]. Pathol Biol (Paris). 1995. 43(5): p. 461-70.
-
Pugashetti, R., et al., Dermal mucinosis as a sign of venous insufficiency. J Cutan Pathol., 2010. 37(2): p. 292-6. doi: 10.1111/j.1600-0560.2009.01306.x. Epub 2009 Jul 10.
-
Hainsworth, R., Arterial blood pressure, in Hypotensive anaesthesia, G.E.H. Henderby, Editor. 1985, Churchill Livingstone,: Edinburgh. p. 3–29.
-
Varaliová, Z., et al., Lymphatic drainage affects lipolytic activity of femoral adipose tissue in women. Int J Obes, 2020. 5(10): p. 020-0559.
-
Szolnoky, G., et al., Complex decongestive physiotherapy decreases capillary fragility in lipedema. Lymphology., 2008. 41(4): p. 161-6.
-
Casley-Smith, J.R. and J.R. Casley-Smith, Modern Treatment for Lymphoedema. Fifth, revised Edition. 1997, South Australia: The Lymphoedema Association of Australia, Inc. 335.
-
Szolnoky, G., et al., Lymphedema treatment decreases pain intensity in lipedema. Lymphology., 2011. 44(4): p. 178-82.
-
Herbst, K.L., C. Ussery, and A. Eekema, Pilot study: whole body manual subcutaneous adipose tissue (SAT) therapy improved pain and SAT structure in women with lipedema. LID – 10.1515/hmbci-2017-0035 [doi] LID – /j/hmbci.ahead-of-print/hmbci-2017-0035/hmbci-2017-0035.xml [pii]. Horm Mol Biol Clin Investig, 2017(1868-1891 (Electronic)).
-
Ibarra, M., et al., Subcutaneous adipose tissue therapy reduces fat by dual X-ray absorptiometry scan and improves tissue structure by ultrasound in women with lipoedema and Dercum disease. Clin Obes., 2018. 8(6): p. 398-406. doi: 10.1111/cob.12281. Epub 2018 Sep 24.
-
Bernardi, J.M. and J. Malone, Thyroid dermopathy localized to areas of injury and responsive to complete decongestive physiotherapy. J Am Acad Dermatol., 2011. 64(6): p. 1219-20. doi: 10.1016/j.jaad.2009.11.014.
-
Langevin, H.M. and J.A. Yandow, Relationship of acupuncture points and meridians to connective tissue planes. Anat Rec., 2002. 269(6): p. 257-65. doi: 10.1002/ar.10185.
-
Li, H., et al., An extravascular fluid transport system based on structural framework of fibrous connective tissues in human body. Cell Prolif., 2019. 52(5): p. e12667. doi: 10.1111/cpr.12667. Epub 2019 Aug 1.
-
Nielsen, A. and T.J. Kaptchuk, Physiology of Gua Sha. 2nd ed. Gua Sha. A Traditional Technique for Modern Practice. 2013, Philadelphia, Pennsylvania: Elsevier Ltd.
-
Mariman, E.C. and P. Wang, Adipocyte extracellular matrix composition, dynamics and role in obesity. Cell Mol Life Sci., 2010. 67(8): p. 1277-92. doi: 10.1007/s00018-010-0263-4. Epub 2010 Jan 27.
-
Tanabe, Y., et al., Inhibition of adipocyte differentiation by mechanical stretching through ERK-mediated downregulation of PPARgamma2. J Cell Sci., 2004. 117(Pt 16): p. 3605-14. doi: 10.1242/jcs.01207.
-
Huff, J.B., et al., Lymphatic pump treatment augments lymphatic flux of lymphocytes in rats. Lymphat Res Biol., 2010. 8(4): p. 183-7. doi: 10.1089/lrb.2010.0009.
-
Hodge, L.M., et al., Abdominal lymphatic pump treatment increases leukocyte count and flux in thoracic duct lymph. Lymphat Res Biol, 2007. 5(2): p. 127-33. doi: 10.1089/lrb.2007.1001.
-
Reed, R.K., et al., Lymphatic Hyaluronan Flux from Skin Increases during Increased Lymph Flow Induced by Intravenous Saline Loading. International Journal of Microcirculation, 1994. 14(1-2): p. 56-61.
-
Ronco, C. and J.A. Kellum, Critical Care Nephrology. 2009, United Kingdom: Saunders/Elsevier.
-
Särnstrand, B., R. Brattsand, and A. Malmström, Effect of glucocorticoids on glycosaminoglycan metabolism in cultured human skin fibroblasts. J Invest Dermatol., 1982. 79(6): p. 412-7. doi: 10.1111/1523-1747.ep12530360.
-
Johnson, D.H., J.M. Bradley, and T.S. Acott, The effect of dexamethasone on glycosaminoglycans of human trabecular meshwork in perfusion organ culture. Invest Ophthalmol Vis Sci., 1990. 31(12): p. 2568-71.
-
McKay, L.I. and J.A. Cidlowski, Physiologic and Pharmacologic Effects of Corticosteroids, in Holland-Frei Cancer Medicine, D.W. Kufe, et al., Editors. 2003: Hamilton (ON).
-
Martin, J.V., D.M. Liberati, and L.N. Diebel, Excess sodium is deleterious on endothelial and glycocalyx barrier function: A microfluidic study. J Trauma Acute Care Surg, 2018. 12(10): p. 0000000000001892.
-
Ehrlich, C., et al., Lymphedema and Lipedema Nutrition Guide. Foods, vitamins, minerals, and supplements. 2016, San Francisco: Lymph Notes.
-
Minich, D.M., A Review of the Science of Colorful, Plant-Based Food and Practical Strategies for “Eating the Rainbow”. Journal of Nutrition and Metabolism, 2019. 2019: p. 2125070.
-
Casley-Smith, J.R. and J.R. Casley-Smith, The effects of diosmin (a benzo-pyrone) upon some high-protein oedemas: lung contusion, and burn and lymphoedema of rat legs. Agents Actions, 1985. 17(1): p. 14-20.
-
Feldo, M., et al., Influence of Diosmin Treatment on the Level of Oxidative Stress Markers in Patients with Chronic Venous Insufficiency. Oxid Med Cell Longev., 2018. 2018:2561705.(doi): p. 10.1155/2018/2561705. eCollection 2018.
-
McGregor, G.P. and H.K. Biesalski, Rationale and impact of vitamin C in clinical nutrition. Curr Opin Clin Nutr Metab Care., 2006. 9(6): p. 697-703. doi: 10.1097/01.mco.0000247478.79779.8f.
-
Tanaka, H., et al., High dose vitamin C counteracts the negative interstitial fluid hydrostatic pressure and early edema generation in thermally injured rats. Burns., 1999. 25(7): p. 569-74. doi: 10.1016/s0305-4179(99)00073-x.
-
Reed, R.K., et al., Control of interstitial fluid pressure: role of beta1-integrins. Semin Nephrol., 2001. 21(3): p. 222-30. doi: 10.1053/snep.2001.21646.
-
Ludwig, J., P. Linhart, and A.H. Baggenstoss, Hepatic lymph drainage in cirrhosis and congestive heart failure. A postmortem lymphangiographic study. Arch Pathol., 1968. 86(5): p. 551-62.
-
Benias, P.C., Wells, R.G., Sackey-Aboagye, B. et al. Structure and Distribution of an Unrecognized Interstitium in Human Tissues. Sci Rep 8, 4947 (2018). https://doi.org/10.1038/s41598-018-23062-6
DISCLAIMER
Lio Lipedema Italia Onlus is grateful to all valuable websites and lipedema sufferers’ associations for all the precious materials
which are generously provided in their social channels to the benefit of all lipedema community worldwide.
Please consider visiting their websites for more info.

